高纯度质粒小提试剂盒
基本售价:240.00元
储存条件 该试剂盒置于室温(15-25℃)干燥条件下,可保存12个月,更长时间的保存可置于2-8℃。2-8℃保存条件下,若溶液产生沉淀,使用前应将试剂盒内的溶液在室温放置一段时间,必要时可在37℃水浴中预热10 min,以溶解沉淀。第一次使用前将RNase A加入溶液P1中,混匀后置于2-8℃保存,可稳定保存12个月以上。单独包装的RNase A 在室温可稳定保存12个月以上。 产品简介 本试剂盒采用碱裂解法裂解细胞,再通过离心吸附柱在高盐状态下特异性地结合溶液中的DNA。离心吸附柱中采用的硅基质材料为本公司新型材料,高效、专一吸附DNA。由于增加了过滤柱,与普通的提取方法相比,本试剂盒可去除杂质蛋白及细胞中其他有机化合物,适用于提取1-5 ml过夜培养的大肠杆菌,质粒提取得率和质量与宿主菌的种类和培养条件,细胞的裂解,质粒拷贝数,质粒的稳定性,抗生素等因素有关。 使用本试剂盒提取的质粒DNA可适用于转染多种细胞及各种常规操作,包括酶切、PCR、测序、连接等实验。 注意事项 请务必在使用本试剂盒之前阅读此注意事项。 1.溶液 P1 在使用前先加入 RNase A(将试剂盒中提供的 RNase A 全部加入),混匀,置于 2-8℃保存。 2.使用前先检查溶液 P2 和 P3 是否出现浑浊,如有混浊现象,可在 37℃水浴中加热几分钟,即可恢复澄清。 3.注意不要直接接触溶液 P2 和 P3,使用后应立即盖紧盖子。 4.所有离心步骤均为使用台式离心机室温下进行离心,速度为 12,000 rpm (~13,400×g)。 5.提取的质粒量与细菌培养浓度、质粒拷贝数等因素有关。 操作步骤 使用前请先在漂洗液PW中加入无水乙醇,加入体积请参照瓶上的标签。 1.取1-5 ml过夜培养的菌液加入离心管中,12,000 rpm (~13,400×g )离心1 min,尽量吸除上清(菌液较多时可以通过几次离心将菌体沉淀收集到一个离心管中)。 2.向留有菌体沉淀的离心管中加入250 μl溶液P1 (请先检查是否已加入RNase A),使用移液器吸吐或涡旋振荡器彻底悬浮细菌细胞沉淀。 注意:如果有未彻底混匀的菌块,会影响裂解,导致提取量和纯度偏低。 3.向离心管中加入250 μl溶液P2,温和地上下翻转6-8次使菌体充分裂解。 注意:温和地混合,不要剧烈震荡,以免打断基因组DNA,造成提取的质粒中混有基因组DNA片断。此时菌液应变得清亮粘稠,所用时间不应超过5 min,以免质粒受到破坏。如果未变得清亮,可能由于菌体过多,裂解不彻底,应减少菌体量。 4.向离心管中加入250 μl溶液P3,立即温和地上下翻转6-8次,充分混匀,此时会出现白色絮状沉淀。12,000 rpm (~13,400×g ) 离心10 min,用移液器小心地将上清转移到过滤柱CS1(过滤柱放入收集管中),注意尽量不要吸出沉淀。 注意:P3加入后应立即混合,避免产生局部沉淀。如果上清中还有微小白色沉淀,可再次离心后取上清。 5.12,000 rpm (~13,400×g )离心2 min,小心地将离心后收集管中得到的溶液转移到吸附柱CP1中(吸附柱放入收集管中),(如果过滤柱中有残余的液体说明步骤4吸取的上清中杂质过多,可以延长离心的时间; 如果离心后收集管底部有少量的沉淀,尽量的吸取上清)。 6.12,000 rpm (~13,400×g ) 离心30-60 sec,倒掉收集管中的废液,将吸附柱CP1放入收集管中。 7.向吸附柱CP1中加入700 μl漂洗液PW(请先检查是否已加入无水乙醇),12,000 rpm(~13,400×g ) 离心30-60 sec,倒掉收集管中的废液,将吸附柱CP1放入收集管中。 8.重复操作步骤7。 9.将吸附柱CP1放入收集管中,12,000 rpm (~13,400×g ) 离心2 min,目的是将吸附柱中残余的漂洗液去除。 注意:漂洗液中乙醇的残留会影响后续的酶反应(酶切、PCR等)实验。为确保下游实验不受残留乙醇的影响,建议将吸附柱CP1开盖,置于室温放置数分钟,以彻底晾干吸附材料中残余的乙醇。 10.将吸附柱CP1置于一个干净的离心管中,向吸附膜的中间部位滴加50-100 μl洗脱缓冲液TB,室温放置2 min,12,000 rpm (~13,400×g) 离心2 min将质粒溶液收集到离心管中。 注意:洗脱缓冲液体积不应少于50μl,体积过小影响回收效率。洗脱液的pH值对于洗脱效率有很大影响,若后续做测序,需使用ddH2O做洗脱液,并保证其pH值在7.0-8.5范围内,pH值低于7.0会降低洗脱效率。且DNA产物应保存在-20℃,以防DNA降解。为了增加质粒的回收率,可将得到的溶液重新加入吸附柱中,室温放置2 min,12,000 rpm(~13,400×g) 离心2 min,将质粒溶液收集到离心管中。 低拷贝或大质粒( >10kb)提取 如果所提质粒为低拷贝质粒或大于10 kb的大质粒,应加大菌体使用量,使用5-10 ml过夜培养物,同时按照比例增加P1、P2、P3的用量,洗脱缓冲液TB应在65-70℃水浴预热,在吸附和洗脱时可以适当的延长时间,以增加提取效率。其它步骤相同。

质粒小提试剂盒-200次
基本售价:544.00元
储存条件 该试剂盒置于室温(15-25℃)干燥条件下,可保存12个月,更长时间的保存可置于2-8℃。2-8℃保存条件下,若溶液产生沉淀,使用前应将试剂盒内的溶液在室温放置一段时间,必要时可在37℃水浴中预热10 min,以溶解沉淀。第一次使用前将RNase A加入溶液P1中,混匀后置于2-8℃保存,可稳定保存12个月以上。单独包装的RNase A 在室温可稳定保存12个月以上。 产品简介 本试剂盒采用碱裂解法裂解细胞,再通过离心吸附柱在高盐状态下特异性地结合溶液中的DNA。离心吸附柱中采用的硅基质材料为本公司新型材料,高效、专一吸附DNA。以下操作步骤适用于提取1-5ml过夜培养的大肠杆菌,质粒提取得率和质量与宿主菌的种类和培养条件,细胞的裂解,质粒拷贝数,质粒的稳定性,抗生素等因素有关。 使用本试剂盒提取的质粒DNA可适用于各种常规操作,包括酶切、PCR、测序、连接、转化、文库筛选、体外翻译、转染一些常规的传代细胞等。 注意事项 请务必在使用本试剂盒之前阅读此注意事项。 1.溶液 P1 在使用前先加入 RNase A(将试剂盒中提供的 RNase A 全部加入),混匀,置于 2-8℃保存。 2.使用前请先检查溶液 P2 和 P3 是否出现浑浊,如有混浊现象,可在 37℃水浴中加热几分钟,即可恢复澄 清。 3.注意不要直接接触溶液 P2 和 P3,使用后应立即盖紧盖子。 4.所有离心步骤均为使用常规台式离心机室温下进行离心,速度为 12,000 rpm(~13,400×g )。 5.提取的质粒量与细菌培养浓度、质粒拷贝数等因素有关。 操作步骤 使用前请先在漂洗液PW中加入无水乙醇,加入体积请参照瓶上的标签。 1.取1-5 ml过夜培养的菌液加入离心管中,12,000 rpm(~13,400×g ) 离心1 min,尽量吸除上清(菌液较多时可以通过多次离心将菌体沉淀收集到一个离心管中)。 2.向留有菌体沉淀的离心管中加入250 μl溶液P1(请先检查是否已加入RNase A),使用移液器吸吐或涡旋振荡器彻底悬浮细菌沉淀。 注意:如果有未彻底混匀的菌块,会影响裂解,导致提取量和纯度偏低。 3.向离心管中加入250 μl溶液P2,温和地上下翻转6-8次使菌体充分裂解。 注意:温和地混合,不要剧烈震荡,以免打断基因组DNA,造成提取的质粒中混有基因组DNA片断。此时 菌液应变得清亮粘稠,所用时间不应超过5 min,以免质粒受到破坏。如果未变得清亮,可能由于菌体 过多,裂解不彻底,应减少菌体量。 4.向离心管中加入250 μl溶液P3,立即温和地上下翻转6-8次,充分混匀,此时将出现白色絮状沉淀。12,000 rpm (~13,400×g )离心10 min。 注意:P3加入后应立即混合,避免产生局部沉淀。如果上清中还有微小白色沉淀,可再次离心后取上 清。 5.将上一步收集的上清液用移液器转移到吸附柱CP1中 (吸附柱放入收集管中),注意尽量不要吸出沉淀。12,000 rpm (~13,400×g)离心30-60 sec,倒掉收集管中的废液,将吸附柱CP1放入收集管中。 6.向吸附柱CP1中加入700 μl漂洗液PW(请先检查是否已加入无水乙醇),12,000 rpm(~13,400×g )离心30-60 sec,倒掉收集管中的废液,将吸附柱CP1放入收集管中。 7.重复操作步骤6。 8.将吸附柱CP1放入收集管中,12,000 rpm (~13,400×g) 离心2 min,目的是将吸附柱中残余的漂洗液去 除。 注意:漂洗液中乙醇的残留会影响后续的酶反应(酶切、PCR等)实验。为确保下游实验不受残留乙醇的影响,建议将吸附柱CP1开盖,置于室温放置数分钟,以彻底晾干吸附材料中残余的乙醇。 9.将吸附柱CP1置于一个干净的离心管中,向吸附膜的中间部位滴加50-100 μl洗脱缓冲液TB,室温放置2min,12,000 rpm (~13,400×g) 离心2 min将质粒溶液收集到离心管中。 注意:洗脱缓冲液体积不应少于50μl,体积过小影响回收效率。洗脱液的pH值对于洗脱效率有很大影响,若后续做测序,需使用ddH2O做洗脱液,并保证其pH值在7.0-8.5范围内,pH值低于7.0会降低洗脱效率。且DNA产物应保存在-20℃,以防DNA降解。为了增加质粒的回收率,可将得到的溶液重新加入吸附柱中,室温放置2 min,12,000 rpm(~13,400×g) 离心2 min,将质粒溶液收集到离心管中。 低拷贝或大质粒( >10kb)提取 如果所提质粒为低拷贝质粒或大于10 kb的大质粒,应加大菌体使用量,使用5-10 ml过夜培养物,同时按照比例增加P1、P2、P3的用量,洗脱缓冲液TB应在65-70℃水浴预热,在吸附和洗脱时可以适当的延长时间,以增加提取效率。其它步骤相同

Vipack 病毒包装转染试剂
基本售价:360.00元
【操作方法】1. 对于贴壁细胞(以下均以6孔板为例,其它培养皿或培养板请根据相应面积换算):a.将细胞培养于培养皿或培养板内,通常在铺板后1-2天内长到70-90%。 b. 在转染前1-2小时,吸去细胞培养液,更换为新鲜的不含抗生素的完全培养液2ml。c. 取2-4μg待转染的质粒DNA (质粒总体积不宜超过20μl,若有多种质粒请混匀),以质量体积比1:3加入转染试剂6~12μl(如2μg待转染的质粒DNA加入转染试剂6μl)。d.混匀后,室温孵育3-5分钟。e. 把DNA-转染试剂混合物中加入500μl opti-MEM(若无opti-MEM可使用无血清无双抗的DMEM或1640,具体根据转染细胞使用的培养基),充分混匀后静置10-15分钟。 f.后均匀滴加到整个6孔板内(加入前吸出原培养板中500μl培养基),并置于含5%二氧化碳的37ºC细胞培养箱内培养。 g. 在转染后4-6小时左右换液,更换为2ml新鲜的完全培养液,继续培养。h.通常在转染约24-48小时后就可以检测到转染基因的表达。2. 对于悬浮细胞: a. 离心收集悬浮细胞,用PBS洗涤一次。 b. 按照上面的步骤c)、d)、e)制备DNA-转染试剂-optiMEM混合物。c. 每106个细胞的沉淀,用500微升DNA-转染试剂-optiMEM混合物重新悬浮,室温放置15-20分钟。 d. 在一个6孔板孔内加入1.5ml完全培养液,然后加入来自上一步的细胞-500微升DNA-转染试剂-optiMEM混合物,混匀。e. 在含5%二氧化碳的37ºC细胞培养箱内培养。 f. 根据实验要求和转染试剂对于不同细胞的毒性不同,在4-6小时后离心收集细胞,用PBS洗一次,然后用2毫升完全培养 液重新悬浮细胞,继续培养。 g. 通常在转染约24-48小时后就可以检测到转染基因的表达。

NewZOL LS 总RNA提取试剂(NewZOL LS Reagent) 200ml
基本售价:890.00元
功能与使用方法与life品牌的Trizol LS相似 【保存条件】2-8℃长期保存【操作方法】I. 样本处理1. 组织样本处理:用匀浆器或其他类似设备匀化组织样本机械破坏装置,每 500μL 最多使用 50 mg 组织NewZOL LS。 对于 DNA 含量高的组织(例如脾脏),建议使用 25 mg 组织/ 500μL 试剂。 2. 贴壁细胞样本处理:除去细胞培养基,通过向培养皿(直径 3.5 cm,10 cm2)中加入至少 1 mL NewZOLLS 并通过反复吸移来确保完全裂解。(根据培养皿面积而不是细胞数计算试剂量。试剂量不足将导致分离的 RNA 受到 DNA 污染。残留的匀浆可以在-20 至-80°C 下保存至少一年,以备后用。) 3. 悬浮细胞样本处理:沉淀细胞,并通过添加 NewZOL LS 直接裂解。 每 5×106个细胞至少加入 500μLNewZOL LS,移液器吹打数次裂解细胞。(添加 NewZOL LS 之前请勿洗涤细胞,细胞洗涤可能会导致 RNA降解。) 4. 液体样本处理:每 200μL 液体样品中加入 500μL NewZOL LS 进行均质化和裂解。对于小于 200μL 的样品体积,请添加 500μLNewZOL LS 并加水至最终体积为 700μL。 5. 富含脂质样本处理:如上所述均质化富含脂质的样品。将样品以 12,000×g 离心 5 分钟。 离心后,样品顶部会出现一层脂肪。用移液器吸头尖端刺穿上层,然后将上清液转移到新管中。 II. RNA 提取1. 每使用 500μLNewZOL LS 的裂解液中加入 200μL 无 RNase 的水至裂解液中。剧烈摇动样品 15 秒钟。在室温下孵育 5 分钟。(对于包含 50 mg 组织/ 500μL NewZOL LS 的样品,建议在室温下孵育 15 分钟。) 2. 在室温下以12,000×g离心样品15分钟。含有DNA,蛋白质和多糖的半固体沉淀物形成在试管底部。RNA仍溶解在上清液中。 3. 将 500μL 上清液转移至新管中。 勿吸太干净防止污染,在 DNA /蛋白质沉淀上方保留一小部分上清液。(含有 DNA,蛋白质和多糖的沉淀物占匀浆-水混合物总量的约 10%。)4. 加入等体积异丙醇,上下颠倒混匀以沉淀 RNA,在室温下孵育样品 10 分钟。5. 将样品以 12,000×g 离心 10 分钟,除去并丢弃上清液。通常,在管的底部以白色沉淀的形式获得 RNA。对于脾脏样品,RNA 在试管底部形成凝胶状膜。用乙醇洗涤后,膜变得更可见。 6. 加入 500μL 75% 乙醇(无 RNase 水配制)洗涤,轻弹管底使沉淀悬浮,上下颠倒混匀。对于较大的试管,按比例添加 75% 乙醇溶液。 7. 将沉淀以 8,000×g 的速度离心 3 分钟。移液去除沉淀中的乙醇,重复乙醇洗涤步骤一次。静置 5-10 分钟待乙醇挥发,无需过份干燥成固体,干燥成固体的 RNA 沉淀不易溶解 8. 将 RNA 沉淀溶于无 RNase 的水中,在室温下涡旋 3 分钟,以实现有效溶解。将得到的 RNA 进行检测或-65℃长期保存(若需更长时间保存请添加适量 RNA Chill(ES-8520))。 【注意事项】1. RNA 酶污染注意事项:a. 提取过程用品均经过去 RNA 酶处理:玻璃制品可以 150 °C 烘烤 4 小时 ,塑料制品可浸泡于 0.5M NaOH 溶液后用清水冲洗并高压灭菌,吸头及离心管类尽量使用一次性无酶吸头及离心管 b. 佩戴手套及口罩及护目镜:皮肤上常含有细菌和霉菌,可污染 RNA 制备,且同时是 RNA 酶来源,同时 New ZOL LS 对皮肤有一定毒性,建议佩戴手套及口罩及护目镜。 c. 尽量于通风橱内提取:避免吸入提取过程中有毒物质。2. 安全性问题:a. 本品在与皮肤接触及吞咽有毒性,可导致烧伤。与皮肤接触后,应立即用洗涤剂和大量水冲洗。如感到身体不适,应立即就医

30-300ul F3 可调八道移液器,半支消毒
基本售价:2250.00元
产品规格:Each准确度:±5.00 to 1.0%Compatible Tips:Finntip:300, Flex 300颜色编码:橙色描述:Finnpipette F3 , 8-ch, 30-300µL通道数:8量程(公制):30-300µL增量:1µL精密度:2.0 to 0.3%
DNA分子量标准 (250-15000 bp) DNA Ladder (250-15000 bp)
基本售价:80.00元
DNA分子量标准 (250-15000 bp) DNA Ladder (250-15000 bp)产品简介:本产品为预混有1×上样缓冲液的即用型DNA分子量标准,由7条线状双链DNA条带组成,适用于对250-15000 bp的双链DNA分子大小的估算和粗略定量。条带组成:250、1000、2500、5000、7500、10000和15000 bp。其中2500 bp条带浓度较大,为20 ng/μl,其余条带浓度约为10 ng/μl。储存液成分:10 mM TrisCl (pH 8.4),10 mM EDTA,0.02%溴酚兰,5%甘油使用说明:1. 建议用于0.5~1.0%的琼脂糖凝胶电泳,不推荐用于聚丙烯酰胺凝胶电泳;2. 电泳缓冲液可选用1x TAE 或0.5~1x TBE,电压6~8 v/cm 胶长,电泳时间30~60分钟;3. 根据上样孔宽度,用灭菌枪头吸取5ul本产品,加入上样孔中;4. 加入待检测DNA 样品后开始电泳;5. 电泳结束后,使用溴化乙啶(EB)或其它DNA 染料染色并观察电泳条带。注意事项:1. 经检测,本品室温放置三个月带型无变化;但建议低温保存,以防因操作不慎导致核酸酶污染而引起条带降解;2. 使用前请勿加热;3. 当电泳缓冲液缓冲能力下降时应及时更换电泳缓冲液,以免影响分辨效果。
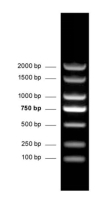
DNA分子量标准 (100-2000 bp) DNA Marker (100-2000 bp)
基本售价:71.00元
DNA分子量标准 (100-2000 bp) DNA Marker (100-2000 bp)产品简介: 本产品为预混有1×上样缓冲液的即用型的稳定、清晰、精准的DNA 分子量标准,由 7 条线状双链 DNA 条带组成,适用于对 100~2000 bp 的双链 DNA 分子大小的估算和粗略定量。条带组成:100、250、500、750、1000、1500、2000bp。其中 750 bp 条带浓度 最大,为 100 ng/5 μl,其余条带浓度约为 50 ng/5 μl 。使用说明:1. 建议用于0.5~1.0%的琼脂糖凝胶电泳,不推荐用于聚丙烯酰胺凝胶电泳;2. 电泳缓冲液可选用1x TAE 或0.5~1x TBE,电压6~8 v/cm 胶长,电泳时间30~60分钟;3. 根据上样孔宽度,用灭菌枪头吸取5~10ul本产品,加入上样孔中;4. 加入待检测DNA 样品后开始电泳;5. 电泳结束后,使用溴化乙啶(EB)或其它DNA 染料染色并观察电泳条带。注意事项:1. 经检测,本品室温放置三个月带型无变化;但建议低温保存,以防因操作不慎导致核酸酶污染而引起条带降解;2. 使用前请勿加热;3. 当电泳缓冲液缓冲能力下降时应及时更换电泳缓冲液,以免影响分辨效果。 PCR Marker
BSA溶液(0.1%,无菌) BSA solution (0.1%, sterile)
基本售价:120.00元
别名:BSA-PBS solution (0.1%, sterile) PBS-BSA溶液(0.1%BSA,无菌)产品简介:平衡盐溶液(Balanced Salt Solution,BSS)与细胞生长状态下的pH值、渗透压等环境状态一致,具有维持渗透压、控制酸碱平衡、供给细胞生存代谢所必需的能量和无机盐成分等作用,可满足体外实验中细胞生存并维持一定的代谢的基本需要。PBS-BSA溶液(0.1%BSA)主要由氯化钠、氯化钾、磷酸氢二钠、磷酸二氢钾、BSA组成,不含Ca2+、Mg2+,pH值为7.4,该试剂经过滤除菌,常用于细胞培养过程中细胞的洗涤或其他常规用途。 本产品仅用于科研领域,不用于临床诊断。
PBS缓冲液 (含5%海藻糖, pH7.2) 1×PBS containing 5 % Trehalose
基本售价:100.00元
PBS缓冲液 (含5%海藻糖, pH7.2) 1×PBS containing 5 % Trehalose别名:PBS containing 5 % Trehalose, pH7.2 磷酸盐缓冲液(1×PBS,含5%海藻糖); 5%海藻糖PBS缓冲液; 5%海藻糖磷酸盐缓冲液;产品简介:本产品为磷酸盐缓冲液(1×PBS)含5%海藻糖,由中性磷酸盐缓冲液与高纯度的海藻糖配制而成,pH: 7.2,海藻糖含量为5%(W/V),是生物学实验常用缓冲液。本产品仅用于科研领域,不用于临床诊断。
中性组织细胞固定液 (10%,NBF) Neutral buffered Formalin,10%
基本售价:200.00元
中性组织细胞固定液 (10%,NBF) Neutral buffered Formalin,10%别名:10% NBF; 固定液; 组织固定液; 组织细胞固定液; 10%福尔马林中性固定液;产品简介:固定的目的在于保存细胞和组织的原有形态结构,固定剂能阻止内源性溶酶体酶对自身组织和细胞的自溶、抑制细菌和霉菌的生长。固定剂通过凝固、生成添加化合物等使蛋白质内部结构发生改变,从而使酶失活。固定剂对细胞核细胞外成分发生物理改变。固定液主要分为醛类固定液、汞类固定液、醇类固定液、氧化剂类固定液、苦味酸盐类固定液等,较为常用的是醛类中的福尔马林、醇类中的乙醇。中性组织细胞固定液 (10%,NBF),更有利于保护超微结构。该法为Carson改良法,主要由甲醛、磷酸盐等组成,其福尔马林含量为10%。使用方法:1. 一般标本固定时间控制在 1~4h/mm,大标本应适当延长固定时间。2. 固定好的组织,可在中性组织细胞固定液 (10%,NBF)或 70%乙醇中长期保存。注意事项:1. 该固定液有一定刺激性和腐蚀性,请在通风较好的环境下小心操作,避免吸入。2. 固定液 pH 最好接近用中性,pH 范围 6~8。3. 组织取材的厚度不同,固定时间也不同。常规活检组织比较适合的厚度为 2~4mm, 一般不超过 6mm。对组织恰当的选材有利于固定液的渗透。4. 固定液的容量应足够,一般固定液与组织块的体积比率应大于 10:1。如果容积不够 大,可以在固定期间更换 1~3 次固定液。5. 温度对固定的影响很明显,提高温度可以加速固定作用,但温度不宜过高。6. 取出新鲜组织后,应及时固定,无法及时固定时,应保存于生理盐水中及时送检。7. 为了您的安全和健康,请穿实验服并戴一次性手套操作。

RIPA裂解液(强) RIPA Lysis buffer (strong)
基本售价:180.00元
RIPA裂解液(强) RIPA Lysis buffer (strong)别名:RIPA buffer(high); RIPA buffer(strong); RIPA buffer; lysis buffer; 蛋白提取试剂盒; 高效组织细胞裂解液; 高效RIPA裂解液(组织/细胞); 蛋白裂解液(组织/细胞);产品简介:RIPA裂解液是一种传统的细胞组织快速裂解液,裂解得到的蛋白样品可用于常规的 Western、IP 等实验。蛋白样品可用BCA Protein Assay Kit (C05-02001) 测定蛋白浓度。由于含有较高浓度的去污剂,不能用Bradford法测定RIPA裂解后的蛋白浓度。RIPA 裂解液种类很多,根据其裂解液的强度不同为强、中、弱三类。为保证实验结果请根据检测样本与检测目的的不同选择适当的裂解液。请参考附件(小助手):各种裂解液的主要特点和差异。RIPA裂解液(强)(Powerful RIPA Lysis Buffer)主要由50mM Tris(pH 7.4),150mM NaCl,1% Triton X-100,1% sodium deoxycholate,0.1% SDS、EDTA 等组成,并含有多种蛋白酶抑制剂成分,可以有效抑制蛋白的降解,维持原有的蛋白间相互作用。含有PMSF(100mM, 100×)一支。本产品仅用于科研领域,不用于临床诊断。

硫酸鱼精蛋白溶液(10%) Protamine sulfate solution (10%)
基本售价:600.00元
硫酸鱼精蛋白溶液(10%) Protamine sulfate solution (10%)产品简介:硫酸鱼精蛋白(Protamine Sulfate)是从鱼类新鲜成熟精子中提取的一种碱性蛋白质的硫酸盐,具有强碱性基团,在生物体内可与强酸性的肝素结合,形成稳定的复合物,从而使肝素失去抗凝能力。此溶液为10%硫酸鱼精蛋白溶液。 本产品仅用于科研领域,不用于临床诊断。

美国通用Rehydragel@LV铝佐剂 Rehydragel@LV Alum Adjuvant
基本售价:400.00元
美国通用Rehydragel@LV铝佐剂 Rehydragel@LV Alum Adjuvant产品简介:Rehydragel®吸附剂氢氧化铝凝胶作为兽医疫苗的辅剂使用已有多年,在人类生物领域的重要性也日益增长。这些高纯度氢氧化铝凝胶在作为兽医抗毒素的基体或载体使用时,可产生高度的蛋白吸附能力。Rehydragel辅剂以矿物学上称为勃姆石的结晶状羟基氢氧化铝为基础。当需要结合带负电的蛋白时,它们在疫苗中是非常有效的。在生理pH值(7.4)和9至12的零电荷点时它们带一个正电荷。它们是含有大表面积(约525m2/g)结晶颗粒的水合凝胶。它们的AI2O3 含量范围为2%至10%。 Rehydragel 系列包括AI2O3浓度很高的经济型产品,以及高度专门化产品。
50×TAE 缓冲液 50×TAE Buffer
基本售价:180.00元
50×TAE 缓冲液 50×TAE Buffer别名:Tris-acetic acid buffer (50×TAE); Tris-acetic acid buffer (50*TAE); TAE Buffer,50×; 电泳用Tris-乙酸(TAE, 50X); Tris-乙酸电泳缓冲液(50×TAE);产品简介:Tris-乙酸电泳缓冲液即Tris acetate-EDTA buffer,简称TAE。1×TAE工作液中含有40mM Tris-acetate、1mM EDTA(pH8.0)。TAE是常用的DNA电泳缓冲液, 本试剂是50倍浓缩的TAE,主要由2M Tris-acetate,50mM EDTA组成,使用时需用蒸馏水或去离子水稀释50倍后使用。 本产品仅用于科研领域,不用于临床诊断。

1M二硫苏糖醇(DTT)溶液 1M DTT solution
基本售价:200.00元
1M二硫苏糖醇(DTT)溶液 1M DTT solution 别名:DTT溶液(1mol/L,RNase free); DTT溶液(1mol/L);产品简介:二硫苏糖醇简称DTT,CAS:27565-41-9,分子式为C4H10O2S2,分子量:154.2。DTT与巯基乙醇作用相似,是巯基化DNA的还原剂和去保护剂,以用于还原蛋白质中二硫键,有抗氧化作用。DTT的刺激性气味和毒性比巯基乙醇低很多。DTT溶液(1mol/L, RNase free)主要由DTT、乙酸钠、DEPC处理水等组成,过滤除菌。蛋白质巯基还原实验DTT的常用工作浓度是1-10 mM。 本产品仅用于科研领域,不用于临床诊断。

苯唑西林溶液 (64mg/ml) Oxacilli (64mg/ml)
基本售价:220.00元
苯唑西林溶液 (64mg/ml) Oxacilli (64mg/ml)产品介绍:苯唑西林(Oxacillin)是一种青霉素类抗生素,为耐青霉素酶青霉素,其抗菌作用方式与青霉素相仿。苯唑西林对产青霉素酶葡萄球菌具有良好抗菌活性,对各种链球菌及不产青霉素酶的葡萄球菌抗菌活性则逊于青霉素G。苯唑西林通过抑制细菌细胞壁合成而发挥杀菌作用。苯唑西林时常被用于分子生物学实验研究中,如用于配制含苯唑西林的LB培养基或LB平板等。 苯唑西林溶液(Oxacillin,64mg/ml) 为无菌溶液,一般工作浓度为0.4~6.4μg/ml,主要用于抗青霉素酶葡萄球菌的培养。 本产品仅用于科研领域,不用于临床诊断。
罗丹明123溶液(0.5mg/ml)
基本售价:150.00元
罗丹明123溶液(0.5mg/ml)Rhodamine123 Solution(0.5mg/ml)Rhodamine123是一种可以通过细胞膜的选择性染色活细胞线粒体的荧光染料,呈黄绿色荧光,多用于检测线粒体膜电位,也常用于细胞凋亡检测。它可以快速通过细胞膜,仅需几分钟就可以被具有活性的线粒体所俘获,并且对细胞没有任何毒性。Rhodamine123还用于对许多种细胞进行染色,包括植物细胞和细菌,由于细胞内ATP的量与Rh123的荧光强度之间有相关性,因此Rh123也被用于检测细胞内的ATP。 本产品仅用于科研,不宜用于临床诊断或其他用途。
 中文
中文